文 | 熊玮
历史上,实体编辑部位于波士顿Longwood区的The New EnglandJournal of Medicine(中文名:新英格兰医学杂志)办刊近210年,推进医学进步,硕果累累曾经获得荣誉无数。最新科学引文索引(SCI)影响因子IF大于70分。
2020年1月24日到31日,一方面这本大名鼎鼎的杂志和英格兰的The Lancet (中文名:柳叶刀)一起刊发了来自中国大陆抗疫新型冠状病毒(2019-nCoV)的顶级学术成果,从基础科研到早期临床流行病学均在十天内火速推向全球业内外公众。
同时,NEJM在1月31日不失时机地以Brief report形式刊发了美国医疗系统的关于新型冠状病毒感染的第一篇临床个案研究报告,其中提到Gilead公司(Gilead Sciences Inc.)处于临床研究阶段的新药——瑞德西韦(Remdesivir )。因本文发表背景正是中国国内公众笼罩于2019-nCoV疫情恐慌情绪下,即刻引发了国内追逐、吹捧,各种公众号、自媒体纷纷庆祝,一时间似乎成为家喻户晓的“明星药”。
本文作者仔细回顾了来自美国华盛顿州西雅图市CDCP的这篇报告——“First Case of 2019 Novel Coronavirus in the United States“ (https://www.nejm.org/doi/10.1056/NEJMoa2001191)至少可肯定:目前为止,瑞德西韦可治疗新型冠状病毒肺炎的证据缺乏。解读如下:
病例简述
1月31日,《新英格兰医学杂志》报道了美国首例2019-nCoV感染患者的诊疗过程和临床特征:患者为一位35岁的男性,1月15日从武汉返回美国后出现咳嗽发热,最终于1月20日确诊为美国首例2019-nCoV感染患者,在空气隔离病房接受了对症支持治疗、抗生素治疗和瑞德西韦药物治疗等一系列治疗后,体温正常,发烧、咳嗽、呼吸困难等症状消失,患者病情出现好转(图3)。这一简述和国内很多媒体转载“美国首例确诊新型冠状病毒肺炎患者成功治愈”是有区别的。
图1 NEJM原文首页
解析实际指导意义
第一,该病例临床病程总体上提示属于轻症病例,且反映了普通型患者的典型临床病程。这名35岁男子且在结束中国武汉之行返回美国后发病、急诊就诊、到经鼻咽/口咽拭子检测2019-nCov阳性后,经CDC指定到华盛顿州Providence区域医疗中心空气隔离病房进行观察治疗。临床症状、病程、指标及X线胸片等均提示属于普通型病例,虽然入院第5天晚上(发病第9天)静息状态氧饱和度降至90%并给予鼻导管吸氧。
毫无疑问,该个案对大部分中国住院患者的指导意义有限。因中国定点医院收治的重型及危重型患者比例更高。中国武汉市金银潭医院和武汉病毒研究所于北京时间1月30日在线发表于《柳叶刀》(The Lancet)(Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)30211-7/fulltext)中国新型冠状病毒(2019-nCoV)感染患者的临床数据,这一组患者样本为99例;其中,合并器官功能损害者(急性呼吸窘迫综合征、急性肾损伤、急性呼吸损伤、脓毒症休克、呼吸机肺炎)占这一组患者群的三分之一(33/99,33%),即:中国定点医院收治危重型患者比例更高。
其中,75例(76%)患者接受抗病毒治疗,包括奥司他韦(oseltamivir)、更昔洛韦(ganciclovir)、以及最近引起广泛关注的抗HIV感染疗法洛匹那韦/利托那韦(lopinavir/ritonavir)。抗病毒治疗时间为3-14天。截至论文统计截止日期(1月25日),99例患者中,31例(31%)患者出院,11例(11%)患者死亡,其他病人仍在住院。
第二,新型冠状病毒感染传播源:各种体腔分泌物及血清均有病毒,但鼻咽病毒量和体温、胸片及肺部症状等临床图景不呈现“简单”直接正相关。
该患者在发病第1-3天出现了咳嗽和自我感觉发热的现象,发病第4天到医院就诊,检测体温为37.2℃,X光胸片显示无异常。从上述临床表征评估,患者仍处于2019-nCoV发病的早期。但临床医生鉴于该患者的武汉接触史以及其他流感病毒检测阴性的情况,对患者进行了新型冠状病毒的RT-PCR检测,检测结果为阳性,且Ct值非常低(Ct值越低表明病毒浓度越高),提示患者发病第4天时的病毒浓度是非常高的,具有较强的传播性。
该患者同时送检了多种样本类型进行核酸检测,包括鼻咽部拭子、口腔拭子、血清、尿液、粪便,检测结果显示鼻咽部拭子与口腔拭子均可检出2019-nCoV,且鼻咽部拭子采样病毒浓度相比口腔拭子更高,血清和尿液检测均为阴性,粪便中也能检出少量新型冠状病毒。鼻咽拭子可能是更好的检测样本,也提示飞沫传播是主要途径之一。
该个案初步证实:新型冠状病毒在早期甚至可能在潜伏期在鼻咽部、口腔部等具有较高病毒RNA,因此具有较强的传播性,在疾病某个时期粪便中也有,提示“粪—手—口传播”途径可能存在,这些病原学分布证据特征与目前国内传染播散模式具有一定吻合。
但图2也提示:鼻咽病毒量和体温、胸片及肺部症状等临床图景不呈现“简单”直接正相关。因此,核酸检测是病原学诊断,不是临床诊断,临床分型治疗要基于临床体征、影像学诊断而非核酸检测结果。
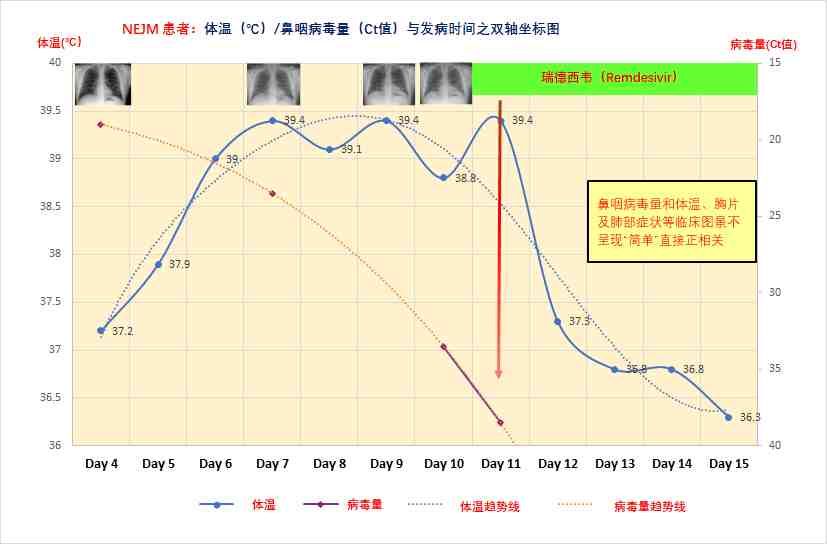
图2 体温、X线胸片、病毒量与发病时间(据原文数据制图)
第三,普通轻症患者治疗以对症处理为主,预防性抗菌素使用视情况而定。
患者入院后,前期的一系列治疗方案均为对症辅助性治疗:2升生理盐水和恩丹西酮缓解恶心呕吐;每4小时服用乙酰氨基酚、每6小时服用布洛芬缓解发热症状;愈创甘油醚和6升生理盐水缓解持续咳嗽。患者在入院第5天(发病第9天)开始出现经X线胸片证实的肺炎,因临床医生担心是院内获得性肺炎,在入院第6天(发病第10天)使用万古霉素和头孢吡肟抗生素治疗,但在2~3天后PCT阴性及MRSA阴性的情况下,均停用两种抗菌素。该例对临床新型冠状病毒感染患者治疗作出重要提醒:2019-nCoV感染可能影响患者免疫功能,导致院内获得性肺炎发生风险,临床治疗中需警惕。
当然,武汉市金银潭医院在《柳叶刀》论文中已报告:多数患者(70/99,71%)接受了抗生素治疗,其中25例(25%)患者接受单一抗生素治疗,45例(45%)患者接受联合抗生素治疗。
第四,瑞德西韦治疗新型冠状病毒疗效证据并不充分,需临床试验进一步验证。
患者在入院第7天(发病第11天)因“2019-nCoV RNA持续阳性”而采用了吉利德公司的一款正处于“试验性特许用药”——RNA聚合酶(RNA-dependent RNA Polymerase,RdRp)抑制剂——瑞德西韦进行治疗,巧合的是用药一天后即入院第8天(发病第12天)临床症状改善。
注意Remdesivir用药时间点:病程中体温接近正常环节;鼻咽部病毒量大幅度下降。而这两点也对此时瑞德西韦的药效确切作用提出质疑,因此,即刻引起巨大轰动的Remdesivir,更应该谨慎地解读该药在这例患者上取得的实际疗效。
从该例患者层面分析,患者年龄为35岁,较为年轻,不排除其自身天然免疫(Innate immunity)作为抗病毒第一道防线在对抗2019-nCoV中发挥作用,病毒检测结果也显示在静脉给予瑞德西韦时(发病第11天),患者病毒浓度相比之前已显著降低(Ct值为33-34),提示用药时患者病毒已处于较低水平。
客观地看上面的图2:在该患者中发病第12天,鼻咽拭纸RNA阳性滴度已显示降低(距离两周自愈时间似乎到了,可能是自然降低),瑞德昔韦此时介入,效果几何值得探讨。

图3 NEJM患者的临床图景
第五,除粉墨登场的明星——瑞德西韦(Remdesivir)外,针对治疗新型冠状病毒的候选药物包括RNA聚合酶(RNA-dependent RNA Polymerase,RdRp)抑制剂和蛋白酶(protease)抑制剂等:瑞德西韦Remdesivir(吉利德Gilead,RNA聚合酶抑制剂)、法匹拉韦(中国海正,RNA聚合酶抑制剂)、洛匹那韦(艾伯维,蛋白酶抑制剂)、奈非那韦(辉瑞Pfizer,蛋白酶抑制剂)等,但均处于临床前研究阶段,但距临床应用尚需时间。
2月2日,钟南山院士在接受了新华社、央视新闻、南方+等媒体的采访,回应多个关于疫情的关键问题。他表示,迄今2019-nCoV还没有针对性的特效药,一些个案报道的治疗药物仍需更多的临床实践证明效果。中国武汉新型冠状病毒毒株(2019-nCoV)以前在人类中从未公开发现,因此,“一切皆在探索中”。宣称“XX或**sivir”等产生“治愈疗效”,除了鼓舞人心的社会心理效果外,也有误导公众嫌疑。
不过,Gilead公司在1月31日的官方声明中很客观表述为:“瑞德西韦尚未在全球任何地方获得许可或批准,尚未证明其任何用途的安全性或有效性。目前只是应治疗医生的要求,并在当地监管机构的支持下,Gilead提供瑞德西韦用于少数2019-nCoV患者,作为紧急治疗。”
在今天下午卫健委举行的新闻发布会上,科技部发言人表示瑞德西韦将于今天下午抵达国内,开展临床试验,我们既要翘首以盼,也要谨慎看待。未来,希望Gilead公司能和中国医疗界一起增加临床研究病例获得治疗2019-nCoV的实质性支撑证据。
药物背景
瑞德西韦是一种由美国吉利德公司设计用于治疗埃博拉病毒(Ebolavirus)和马尔堡病毒(Marbergvirus)等丝状病毒属(Filoviruses)引发的出血热病毒感染的药物。因2013-2016年西非埃博拉病毒流行,这个药走上快速通道。
2019年9月,在西非刚果进行的现场临床试验——PALM研究结果发现:和单克隆抗体相比,瑞德西韦无效,试验提前终止,基本上停滞了瑞德西韦获得FDA批准的可能,吉利德公司亦终止瑞德西韦的进一步研发进程,即该药在埃博拉病毒治疗领域已被宣判死刑。
参考来源:
1. Holshue ML, DeBolt C, Lindquist S, et al. First Case of 2019 Novel Coronavirus in the United States. N Engl J Med, 2020. https://www.nejm.org/doi/10.1056/NEJMoa2001191
2. Chen N, Zhou M, Dong X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. The Lancet, 2020. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)30211-7/fulltext
3. 国家卫健委.新型冠状病毒感染的肺炎诊疗方案(试行第四版).2020-1-27。
4. 国家卫健委.新型冠状病毒感染的肺炎诊疗方案(试行第五版).2020-2-3.
5. New antibodies best ZMapp in Ebola trial. https://doi.org/10.1038/s41587-019-0284-y
6. 21世纪经济报道、CNBC等.
-
梦之彼方作者
-
邹全作者
-
winter
-
wT#作者
-
慢慢作者
-
高建林
-
穿铁大王爸爸🐖
-
柠檬配蜂蜜作者
-
殳木
-
Rel.Principle.F
-
Apco·hanayo
-
Pansage🐒🍃
-
他山之石(Eric)作者
-
aLexSoLiD作者
-
袁作者
-
The Dark Knight
-
Samhero
-
盀冭
-
宝玉
-
胡子-初
-
靳希军
-
Татьяна
-
刑天不败
